


INVIMA: Nuevos lineamientos para el reporte de eventos adversos en la plataforma VigiFlow©
INVIMA: Nuevos lineamientos para el reporte de eventos adversos en la plataforma VigiFlow©
El Instituto Nacional de Vigilancia de Medicamentos y Alimentos – Invima, informa a las direcciones territoriales de salud, profesionales de las instituciones prestadoras de salud, establecimientos farmacéuticos, y a todos los que pertenecen a la Red Nacional de Farmacovigilancia del Invima, que a partir del mes de septiembre del 2021, se emiten los lineamientos de articulación del Programa Nacional de Farmacovigilancia para el reporte de eventos adversos a través del sistema VigiFlow®, de acuerdo con la circular externa N.º 3000-0526-2021.
Este sistema estará funcionando como la base de datos del Centro Nacional de Farmacovigilancia del Invima, encargado también del envío de reportes a la Organización Mundial de la Salud – OMS, y de la base de datos de las direcciones territoriales de salud, para el estudio y gestión de los reportes.
Es de anotar, que el objetivo principal del Programa Nacional de Farmacovigilancia es vigilar la seguridad, efectividad y calidad de los medicamentos y vacunas, luego de obtener la autorización por parte del Invima. De esta manera, el Programa detecta reacciones adversas, complicaciones no evidenciadas durante la etapa de investigación de los medicamentos y usos inapropiados, entre otros.
A continuación se presentan los lineamientos para iniciar el reporte de eventos adversos en la plataforma:
1. Solicitud y activación de usuario en VigiFlow®
- Las IPS públicas y privadas que tengan habilitado el servicio farmacéutico o aquellas que en la prestación de servicios de salud contemplen la prescripción, la dispensación o la administración de medicamentos, así no tengan habilitado el servicio farmacéutico, incluyendo aquellas IPS del régimen de excepción o con objeto social diferente, tendrán acceso directo al sistema VigiFlow®.
Para tener ese acceso, deberán realizar, aprobar y certificar la capacitación brindada por el Invima, a través del Aula Virtual del Instituto, que encontrarán en el siguiente enlace. - Las instituciones informarán a la dirección territorial de salud, la inscripción en la Red Nacional de Farmacovigilancia mediante el código PNF y remitirán el respectivo certificado de aprobación del Curso: “VigiFlow®-Programa Nacional de Farmacovigilancia -MedDRA”. Si no han efectuado la inscripción a la Red Nacional de Farmacovigilancia, se podrá realizar a través del siguiente enlace.
- Las IPS contarán con un usuario en VigiFlow® que les será asignado por una única vez, independiente del profesional de la salud referente del Programa de Farmacovigilancia institucional.
- Las IPS que cuenten con diferentes sedes a nivel nacional, deberán solicitar un acceso a VigiFlow® por cada sede, a cada dirección territorial de salud de la jurisdicción respectiva, con una cuenta de correo electrónico institucional diferente en cada una.
- La dirección territorial de salud debe priorizar las solicitudes de activación de usuarios de VigiFlow®, a las IPS con servicio farmacéutico y servicio de vacunación habilitado y a los reportantes activos.
- Invima notificará la activación del usuario en VigiFlow® a los correos electrónicos institucionales registrados por las IPS a las direcciones territoriales de salud. Los envíos se realizarán desde el correo: reportefv@invima.gov.co
- Finalmente, la IPS deberá culminar el proceso de activación de usuario, según el tutorial remitido vía correo electrónico, ingresando al sistema de reporte en línea – VigiFlow®, disponible en el siguiente enlace.
2. Tiempos de reporte y términos de transición a VigiFlow®
- La plataforma de reporte en línea SIVICOS, para reporte de eventos de farmacovigilancia, quedará deshabilitada en abril de 2022 y estará disponible solo para la actualización a la Red Nacional de Farmacovigilancia, cierre de casos en seguimiento y consulta de reportes. Por lo tanto, una vez tengan habilitado el usuario de VigiFlow®, deberán realizar el reporte en dicho aplicativo y no a través de la plataforma de reporte en línea SIVICOS manteniéndose, para medicamentos, los tiempos de notificación establecidos en la Resolución 1403 de 2007.
3. Gestión de los reportes por parte de las direcciones territoriales de salud
- Contar con un profesional de salud que coordine las acciones en el ámbito de la farmacovigilancia y este a su vez, deberá contar con un equipo de trabajo de apoyo conformado por perfiles profesionales y académicos complementarios al suyo, con fortalezas específicas en el área de la salud como, por ejemplo, en medicina, química farmacéutica, enfermería, farmacología, epidemiología y toxicología
3.1 Consideraciones respecto al reporte de eventos adversos posteriores a la vacunación (EAPV) en el marco del Plan Nacional de Vacunación contra covid-19
- Todo EAPV grave, detectado por el médico tratante de la institución, debe ser reportado en SIVIGILA del INS, de conformidad con el artículo 6° del Decreto 601 de 2021.
- Los EAPV no graves se reportarán a través de VigiFlow®, durante un espacio de 7 días hábiles para la notificación, desde el momento de la identificación del caso. Lo anterior, en cumplimiento del artículo 5° del Decreto 601 de 2021.
Gestión de reportes medicamentos de control – Fondo Nacional de Estupefacientes
Invima durante el seguimiento y monitoreo de los reportes relacionados con medicamentos de control especial, remitirá al Fondo Nacional de Estupefacientes, los casos que hayan sido notificados por los actores de la Red Nacional de Farmacovigilancia, relacionados con estos medicamentos de control, posterior a finalización de evaluación por parte de las direcciones territoriales de salud.
Por otra parte, para los demás actores, como lo son pacientes y/o cuidadores, establecimientos farmacéuticos mayoristas, establecimientos farmacéuticos minoristas (droguerías y farmacias), establecimientos farmacéuticos independientes definidos por el Invima según su operación logística, transporte especial de pacientes, profesionales independientes de salud, laboratorios clínicos independientes de una IPS, ópticas independientes, clínicas odontológicas, centro de reconocimiento de conductores, IPS de salud ocupacional, IPS que prestan servicios de salud de consulta externa en medicina general y especializada, fisioterapia, fonoaudiología y optometría, no deberán tramitar la generación de usuario en VigiFlow®. Sin embargo, a partir de la fecha de expedición de la circular, podrán realizar el reporte de eventos adversos a través de la interfaz e-Reporting-paciente, ingresando en la página web del Invima, mediante el siguiente enlace.
Finalmente, en caso de presentarse alguna variación en los enlaces señalados en la presente comunicación, Invima informará oportunamente a través de su página web. Adicionalmente, los instructivos estarán disponibles en el micrositio de Farmacovigilancia de la página web del Instituto.
Así mismo, ante cualquier novedad que se presente en el proceso de reporte de los eventos adversos relacionados con medicamentos incluidas las vacunas a través del sistema VigiFlow®, podrá reportarla inmediatamente al correo electrónico: reportefv@invima.gov.co con el Asunto: Novedad reporte VigiFlow®.
MINSALUD: Resolución 200 de 2021. Disposiciones para el uso y manejo de las pruebas utilizadas en el Punto de Atención del paciente POCT
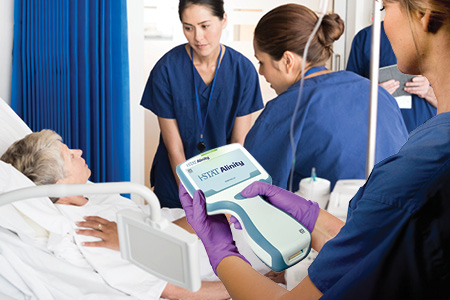
MINSALUD: Resolución 200 de 2021 Disposiciones para el uso y manejo de las pruebas de Laboratorio POCT
Point of Care Testing (POCT, en sus siglas en inglés) se refiere al uso de pruebas de diagnóstico en el punto de atención; es decir son pruebas médicas que se realizan en el sitio donde está el paciente (o cerca de él), pudiendo realizarse en el consultorio de su médico tratante, en su centro de trabajo o, incluso, en su domicilio. El propósito de este tipo de pruebas es proveer de información inmediata al personal de salud, para la toma de decisiones referentes al diagnóstico y tratamiento del paciente.
¿Cuáles son los beneficios de las pruebas Point of Care?
- Pueden conducir a tratamientos médicos más eficientes y efectivos.
- En el hogar, posibilitan que las pruebas sean más frecuentes y consistentes para el control de enfermedades crónicas, como la diabetes.
- Son cruciales para la toma de decisiones inmediatas en situaciones de emergencia y en el quirófano.
- Ayudan a aliviar la congestión en las salas de urgencia al reducir el tiempo que se tarda en tratar a las personas y, por lo tanto, acortar sus estancias.
- Pueden ser útiles en situaciones de desastre o en cualquier escenario que impida el acceso a la electricidad, al agua y a la infraestructura necesaria para las pruebas en un laboratorio.
- Cuando se utilizan en el consultorio médico, pueden reducir las visitas para lectura de resultados o de seguimiento.
- Ayuda a evitar el ausentismo que se produce para la lectura de resultados luego de las pruebas de laboratorio convencionales. Este tipo de pruebas permiten que, por ejemplo, pacientes con VIH obtengan sus resultados de inmediato y no deben regresar para empezar a recibir tratamiento.
- Estas pruebas permiten la atención médica inmediata en zonas rurales y de difícil acceso, donde no existen las condiciones necesarias para implementar laboratorios.
Entre las pruebas que se pueden realizar con este procedimiento destacan:
- Pruebas de glucosa en sangre.
- Análisis de coagulación rápida.
- Marcadores cardíacos rápidos.
- Detección de abuso de drogas.
- Test de tiras de orina.
- Análisis de sangre.
- Diagnóstico de hemoglobinas.
- Pruebas de enfermedades infecciosas.
- Medidas de colesterol.
3. Se determinan los requisitos de formación continua del Talento Humano en Salud y los gestores comunitarios en salud.
4. Se determinar los procedimientos de control de calidad internos y externos
5. Se consagra la obligación de llevar registros documentales para el implementador, y de rerpotar los eventos e incidentes adversos.
BIOINPRO DIAGNOSTICA S.A.S, cuenta con una solución completa para la implemetación de las pruebas POCT que incluye equipos en modalidad de venta o comodato, reactivos y controles de calidad internos y externos.

HPLC: La importancia de medir HBA1C por el método de Referencia Internacional
LA IMPORTANCIA DE MEDIR HBA1C POR EL MÉTODO DE REFERENCIA INTERNACIONAL
La prueba de hemoglobina glicosilada por HPLC está al alcance de cualquier laboratorio. Aquí, algunos aspectos técnicos, metodologías y tecnologías disponibles.
La HbA1c está disponible como prueba de laboratorio para uso clínico desde finales de la década de los 70. Pero no fue hasta los 90 que cobró protagonismo en el control de la diabetes, cuando se demostró su utilidad a partir de dos grandes estudios: el ensayo para complicaciones y control de la diabetes (DCCT, por su sigla en inglés) en pacientes con diabetes tipo 1 y el estudio prospectivo de diabetes del Reino Unido (UKPDS, por su sigla en inglés) en pacientes con diabetes tipo 2.
Estandarización en la medición de HbA1c
En 1992, el Colegio Americano de Patólogos publicó un estudio que mostraba la gran variabilidad analítica de la prueba en ese momento; en los diferentes laboratorios clínicos se podían obtener resultados tan dispares para la misma muestra que iban del 4 al 8,1 %, pudiendo ubicar a un mismo paciente en un nivel de normoglucemia, o directamente en el rango de diabetes.
Como respuesta a esa situación y ante la necesidad de tener una prueba suficientemente confiable, la Federación Internacional de Química Clínica (IFCC, por su sigla en inglés) creó un grupo de trabajo con el objetivo de estandarizar la medición de la HbA1c, incluyendo la preparación y evaluación de material de referencia y el desarrollo de un método de referencia internacional.
En 2007 se publicó la Declaración de Consenso. Posteriormente en 2010, la Asociación Americana de Diabetes (ADA, por su sigla en inglés), gracias a la estandarización y la madurez que alcanzó la prueba, la incorporó como criterio diagnóstico de diabetes, consenso que fue ratificado posteriormente.
Aspectos técnicos relacionados
Determinar con qué instrumento y con cuál metodología medir la concentración de HbA1c es una decisión de suma importancia que implica una gran responsabilidad por parte del laboratorio clínico, más aún, teniendo en cuenta que en el mercado del diagnóstico in vitro hay una amplia gama de alternativas, las cuales varían en cuanto a la tecnología utilizada, el desempeño analítico y el grado de automatización, circunstancias que impactan en la calidad analítica del resultado y en el costo de la prueba.
El conocimiento de los aspectos tecnológicos es de vital importancia para tener pruebas confiables y aplicables a los pacientes, y por esto debe ser analizado al máximo por los profesionales del laboratorio clínico, responsables de que las pruebas sean de óptima calidad, y con la mejor relación costo- beneficio.
En el caso de la HbA1c no hay que perder de vista las recomendaciones del Comité de Expertos Internacionales y la ADA en el sentido de que, para que la prueba pueda ser utilizada como criterio de diagnóstico, debe ser realizada en un laboratorio clínico que utilice instrumentos y reactivos certificados por el Programa Nacional de Estandarización de Glicohemoglobina (NGSP, por su sigla en inglés) y estandarizados de acuerdo con las especificaciones del DCCT.
Metodologías disponibles
En la práctica, definir con cuál método y con qué reactivos trabajar depende de muchos factores sobre los cuales debe primar el desempeño analítico, con resultados precisos y exactos.
Los métodos para medir la concentración de HbA1c se basan en diferencias entre las moléculas la hemoglobina glicosilada y hemoglobina no glicosilada, ya sean físicas, químicas o inmunológicas. (ver gráfica 1)

Los métodos cromatográficos se subdividen en dos grandes grupos diametralmente diferentes: la cromatografía de columna y la cromatografía líquida de alta eficiencia/eficacia (HPLC, por su sigla en inglés).
En los últimos años, los métodos basados en la cromatografía de columnas fueron sustituidos por sistemas automatizados más sólidos entre los que se destaca la cromatografía líquida de alta eficiencia.
El método de HPLC fue el utilizado por el DCCT y se convirtió en el método de referencia. La comunidad científica especializada en diabetología considera a la HPLC como el ‘Gold Standard’ para la determinación cuantitativa de HbA1c en sangre entera. Partiendo de las diferencias estructurales que hay entre la hemoglobina glicosilada en general, la HbA1c en particular, y la Hb0, es posible separar y cuantificar estas fracciones.
Este método no se afecta por el pH ni la temperatura, como tampoco se altera por la presencia de hemoglobinopatías o falla renal por la presencia de hemoglobina carbamilada, ni por la fracción lábil de la hemoglobina glicada, por lo cual es considerado como el método de referencia para la medición de la HbA1c [11].
Estos sistemas utilizan una columna para eluir la muestra en diferentes fracciones: HbA1a, HbA1b, HbA1c y HbA0, sucesivamente, utilizando distintos tampones/buffers con diferente fuerza iónica y pH. Este método presenta una excelente precisión y permite una separación rápida de la HbA1c. (ver gráfica 2)

Un inconveniente que subsistía hasta hace poco tiempo era que el alto costo de los equipos y su funcionamiento sólo lo podían soportar los laboratorios grandes o instituciones de investigación.
De acuerdo con los organismos internacionales relacionados con la diabetes, los laboratorios clínicos europeos muestran una imagen en donde el 70 % de ellos utiliza HPLC, 25 % métodos inmunológicos, y unos pocos cromatografía de afinidad. En nuestro medio no se conoce la proporción, pero ahora está disponible toda esta tecnología y al alcance de la mayoría de los laboratorios.
Es muy importante que los laboratorios clínicos en la medida de sus posibilidades y a la mayor brevedad posible, puedan migrar a metodologías certificadas.
Nuevas tecnologías en el mercado: Equipo D-10 Biorad

El Sistema D-10 para Ensayos de Hemoglobina Glicosilada desarrolla un alto desempeño en un analizador pequeño. Esto provee de un sistema totalmente automatizado el cual combina el monitoreo de diabetes y pruebas de B-talasemia en una sola plataforma. Programado para ensayos rápidos de HbA1c or HbA2/F/A1c mediante una pantalla tactil y puede ser fácilmente integrado en su flujo de trabajo actual en el laboratorio. D-10 con cargador estilo bandeja permite cargar más de 50 muestras para un verdadero analisis sin la intervención de un usuario. Esta capacidad incrementada permite al D-10 crecer al ritmo que el volumen de muestras crece. Con resultados continuos de alta calidad para el monitoreo de la diabetes y pruebas de B-talasemia, el analizador D-10 es la solución para las necesidades de pruebas de hemoglobina glicosilada
Conclusión
La medición de la HbA1c es un eje central tanto en el control de los pacientes con diabetes, ya que de acuerdo con sus valores se han establecido las metas de control y tratamiento, como en el control de las complicaciones a mediano y largo plazo.
La HPLC fue el método utilizado por el DCCT y es considerado el ‘Gold Standard’ por su alta precisión, con un CV menor al 1 % y resultados más confiables, cobrando principal importancia en aquellos que se encuentran alrededor de 6,5 % de HbA1c, valor que la ADA ha establecido como punto de corte para el diagnóstico de diabetes, y que solo recomienda realizar mediante esta metodología.
Los laboratorios clínicos deben realizar los cambios necesarios para alcanzar las metas de desempeño analítico, participando activamente en programas de calidad a nivel nacional e internacional para cumplir el requerimiento de los organismos internacionales, como es la instrumentación y los materiales utilizados certificados por el NGSP y estandarizados según las especificaciones del DCCT.
Tomado de la revista argentina de laboratorio clínico y bioquímica molecular Bioreview, edición 76.
Artículo proveniente de la edición impresa de Octubre – noviembre de 2019 de El Hospital con el código EH1019HBA1C

